如何定量分析组蛋白丙酰化水平?
-
你是否使用了会引入丙酰基的衍生化步骤?
-
如果使用了,是否有同位素区分、替代封闭策略或数据层面的区分方案?
-
你最终比较的是天然位点信号,还是包含实验修饰的总响应?
-
不直接照搬标准丙酸酐流程来回答天然丙酰化定量问题。
-
评估是否采用替代封闭化学、同位素编码策略或不同酶切设计。
-
在方法学说明中明确哪些修饰来自生物样本,哪些来自实验步骤。
-
归一化到总组蛋白量或对应 histone family 信号。
-
在同一肽段家族内比较不同修饰态分数。
-
使用内标肽、QC 样或 pooled sample 评估批次稳定性。
关键要点
|
关键问题 |
简短结论 |
|---|---|
|
组蛋白丙酰化定量是否只能靠 Western blot? |
不能,WB 更适合看总趋势,不能替代位点级定量 |
|
位点级相对定量的核心方法是什么? |
组蛋白富集结合高分辨率 LC-MS/MS |
|
最容易被忽略的误差来源是什么? |
化学 propionylation 衍生化、装载量差异和批次效应 |
|
什么时候要上靶向质谱? |
候选位点少、结论关键、需要重复验证时 |
|
定量结果怎么更可信? |
做好归一化、技术重复、QC 与正交验证 |
|
最重要的实验前提是什么? |
先明确自己要测的是总水平、位点相对丰度,还是特定位点绝对或准绝对丰度 |
什么是组蛋白丙酰化水平定量分析?
组蛋白丙酰化水平定量分析,指的是比较不同样本、处理条件或时间点之间,组蛋白丙酰化的丰度变化。这个“丰度”可以指三种不同层级:
1、总组蛋白或总核蛋白中的整体丙酰化信号强弱。
2、某一条组蛋白肽段或某个位点的相对丰度变化。
3、少数关键位点在标准化条件下的高重复、可比较定量读数。
很多项目之所以一开始就跑偏,不是因为仪器不够好,而是因为把这三种问题混在一起。比如 pan-Kpr 抗体信号升高,只能说明整体趋势变了,不等于 H3K23pr 或 H4K8pr 一定升高;而某个位点在 discovery 数据里出现 fold change,也不等于已经完成了高可信定量验证。
相关服务
定量前,先确定你要回答哪一类问题
1. 只想判断处理前后总水平有没有变化
这类问题更接近筛查。通常关心的是某种刺激、药物、缺氧或代谢条件变化后,组蛋白丙酰化整体是否上升或下降。常用读数包括:
(1)pan-propionylation Western blot 或 dot blot。
(2)组蛋白免疫荧光或免疫组化的相对信号。
(3)以总组蛋白提取物为对象的初步相对定量。
这类方法的优势是快、样本要求相对低,适合做条件摸索;但它回答不了“是哪个位点变了”,也很容易受到抗体特异性和装载量差异影响。
2. 想知道哪些位点发生了相对丰度变化
这类问题属于位点级相对定量,通常要回到组蛋白提取加 LC-MS/MS。它适合做 discovery,帮助你在多个候选位点中找到最值得继续验证的目标。
3. 想把少数关键位点测得更稳、更可重复
如果研究结论最终要落在 1 到 5 个关键位点上,或者需要跨批次、跨样本集比较,靶向质谱往往更合适。PRM 可以在更聚焦的检测窗口里提高重复性和定量稳定性,也更适合后续和功能实验联动。
为什么组蛋白丙酰化定量比普通 PTM 更容易出偏差?
1. 天然丰度通常较低
相较于更常见的乙酰化,天然组蛋白丙酰化在很多模型中的信号更弱,更容易被背景肽段、离子抑制和样本损失放大误差。
2. 组蛋白肽段高度密集且多修饰共存
组蛋白 N 端富含赖氨酸位点,一条肽段上可能同时存在甲基化、乙酰化、丙酰化等多种修饰。对定量来说,这意味着你不仅要测“有多少”,还要先分清“测到的到底是不是同一种东西”。
3. histone bottom-up 工作流本身就可能引入丙酰化
这是最关键的特殊点。传统组蛋白 bottom-up 方法常用丙酸酐对未修饰赖氨酸和肽段 N 端做化学封闭,以便生成更适合色谱和质谱分析的肽段。但当你的研究对象正好是“天然 propionylation”时,这一步会带来解释风险:实验引入的化学丙酰化,可能和内源性丙酰化在质量上相同或极其接近。因此,做定量时必须在方法设计阶段就回答清楚:
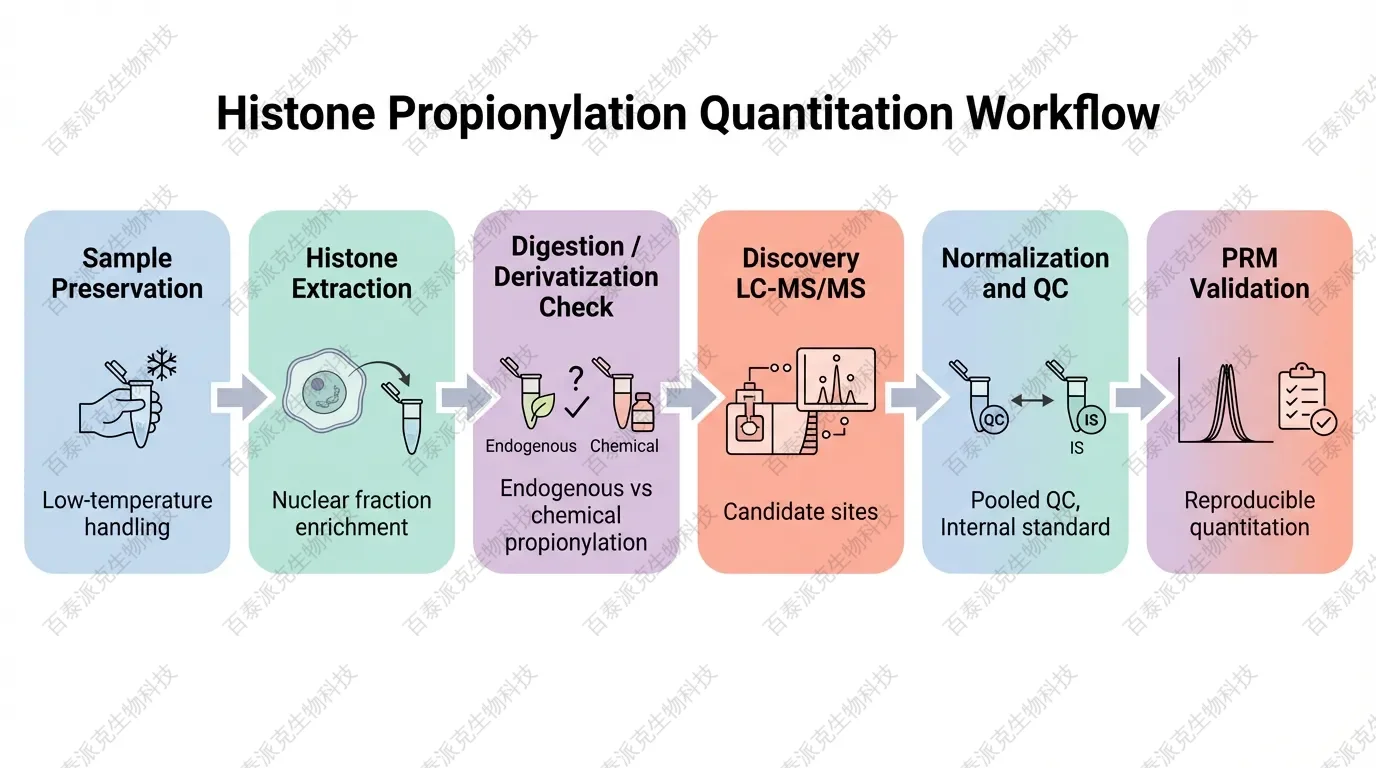
更稳妥的实验流程怎么搭?
第 1 步:保护天然修饰状态
样本进入实验流程后,第一原则不是“尽可能多提蛋白”,而是尽量保住天然修饰谱。常见做法包括低温快速操作、缩短裂解时间、优先获得细胞核或组蛋白组分,以及根据模型加入合适的抑制剂体系。
第 2 步:先把组蛋白组分做干净
如果直接在全蛋白背景中看低丰度丙酰化,误差通常很快放大。更稳妥的策略往往是先做核蛋白富集、酸提组蛋白,必要时进一步分离不同组蛋白组分,再进入酶切与上机。
第 3 步:谨慎选择酶切和衍生化方案
对一般 histone PTM,propionylation derivatization 是成熟方案;但对“天然组蛋白丙酰化定量”本身,这一步要格外谨慎。实践中更可取的思路通常是:
第 4 步:用 discovery LC-MS/MS 找候选位点和变化方向
高分辨率 Orbitrap 类平台配合 nanoLC-MS/MS 仍然是发现阶段的核心。你要的不只是检出,而是能对多修饰肽段做较可靠的定性与相对定量。
第 5 步:把关键位点转入靶向验证
当 discovery 结果筛出少数高价值位点后,再用 PRM 或类似靶向策略做重复验证,通常更容易获得可以支撑结论的定量结果。
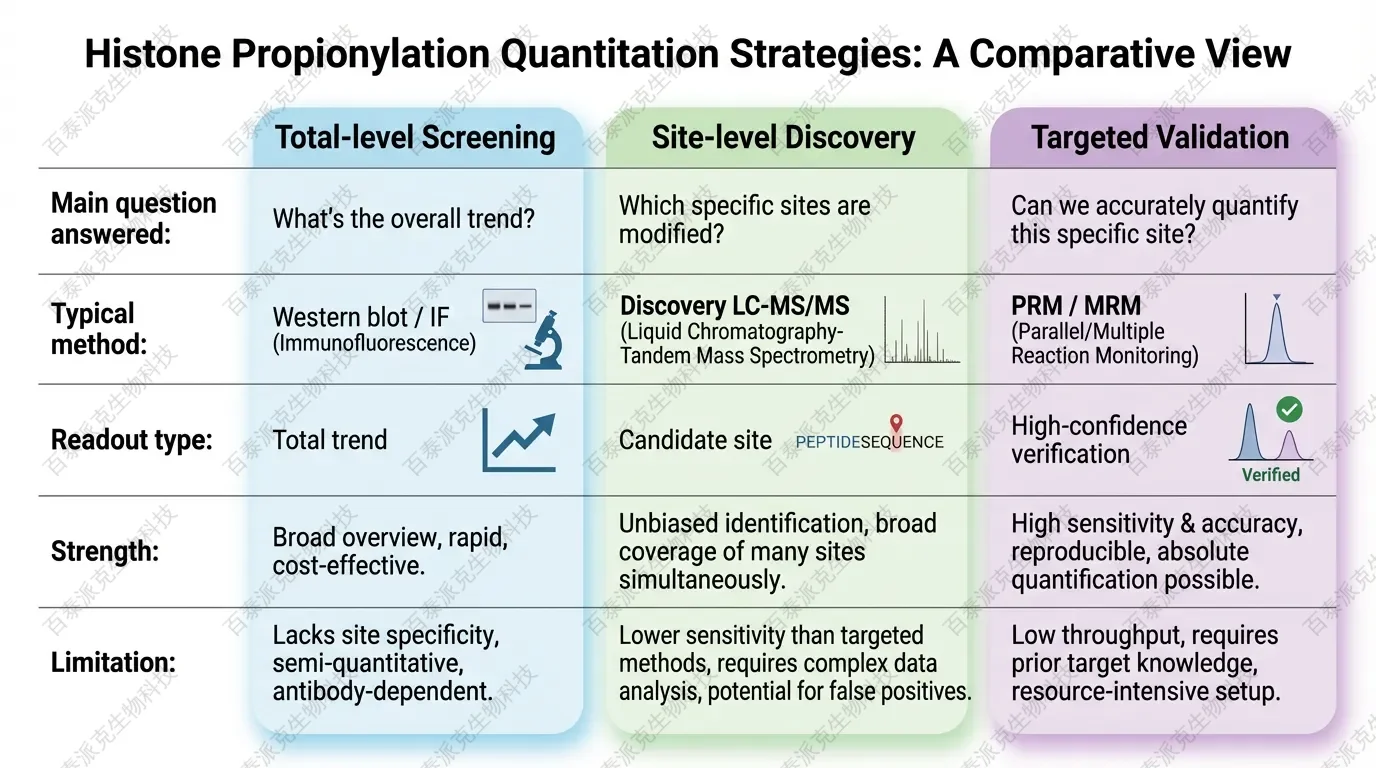
方法选择表
|
方法 |
适合回答的问题 |
主要优势 |
主要限制 |
|---|---|---|---|
|
Western blot / Dot blot |
总组蛋白丙酰化是否变化? |
快,适合条件筛查 |
抗体依赖强,不能给出位点信息 |
|
免疫荧光 / IHC |
某类细胞或组织区域中信号是否变化? |
可结合空间信息 |
更像半定量,受染色条件影响大 |
|
Discovery LC-MS/MS |
哪些位点发生相对变化? |
能做位点级发现 |
前处理和数据分析要求高 |
|
PRM / MRM |
少数关键位点变化是否稳健? |
重复性更好,便于验证 |
依赖已知候选位点 |
|
加内标的 targeted workflow |
能否做更严格的比较定量? |
更利于跨批次比较 |
标准品和方法开发成本更高 |
定量结果最容易在哪些环节失真?
1. 装载量和输入量不一致
如果不同样本进入实验流程的核蛋白量、组蛋白回收量或上样量差异较大,后面的任何相对定量都容易被带偏。总水平方法尤其容易受这个问题影响。
2. 只比较原始峰面积,不做合理归一化
对位点级定量来说,原始峰面积本身不等于可比较结果。更合理的做法常包括:
3. 把 discovery fold change 直接当成最终结论
Discovery 数据更适合做筛选,不适合在没有复核的情况下直接下机制结论。尤其当位点信号弱、缺失值多或重复间波动大时,单次发现结果很容易高估差异。
4. 忽略批次效应和仪器漂移
如果样本数量较多,必须考虑随机上机顺序、穿插 QC、技术重复和批次校正。对低丰度 PTM,仪器状态波动带来的影响往往比普通蛋白定量更明显。
归一化怎么做更合理?
1. 总水平检测
如果采用 Western blot 或 dot blot,通常建议至少做两层控制:
(1)归一化到总 histone H3 / H4 或总组蛋白染色信号。
(2)确认不同样本提取和转膜效率没有系统偏差。
2. 位点级相对定量
如果采用 LC-MS/MS,常见思路是把某个位点的修饰肽段信号,放到同类组蛋白背景或同一肽段的不同修饰态框架中解释,而不是孤立看一个峰面积。
3. 靶向验证
如果进入 PRM/MRM,更推荐引入稳定同位素内标、固定 QC 样和预先定义的接受标准,例如保留时间偏差、离子对一致性和峰形质量。
哪种方案更适合你的项目?
场景 1:你只需要判断处理是否引起整体变化
先做抗体法筛查通常更经济。只要你明确它回答的是“总水平趋势”,而不是“位点结论”,这一步很有价值。
场景 2:你需要发掘新位点或建立变化谱
优先做 discovery LC-MS/MS。它最适合回答“哪些位点可能值得关注”。
场景 3:你已经有候选位点,需要更稳健的结论
尽快转到 PRM 或其他 targeted workflow。尤其当文章核心结论只依赖少数位点时,靶向验证的价值通常最高。
|
项目目标 |
更合适的主路线 |
原因 |
|---|---|---|
|
快速看有无变化 |
抗体法 + 组蛋白装载校正 |
成本较低,适合预实验 |
|
找候选位点 |
组蛋白提取 + discovery LC-MS/MS |
能提供位点级信息 |
|
验证关键位点 |
PRM/MRM + 内标 + QC |
重复性和可解释性更强 |
|
做跨批次比较 |
靶向质谱或严格标准化 workflow |
更容易控制系统误差 |
为什么很多项目最后还是要回到靶向验证?
1. 候选位点少,但结论分量很重
如果论文最终会落在 H3 或 H4 上的少数关键位点,发现型数据通常还不够,靶向验证更能说明这个变化是否稳定。
2. 低丰度位点更容易受随机波动影响
对接近检测下限的信号,靶向采集更容易提高数据一致性,也更便于人工核查碎片和峰形。
3. 需要和功能实验闭环
无论是药物处理、代谢干预还是位点突变实验,真正决定后续实验设计的,往往不是“有没有趋势”,而是“这个位点的变化是否足够可信,可以作为下游假设的锚点”。
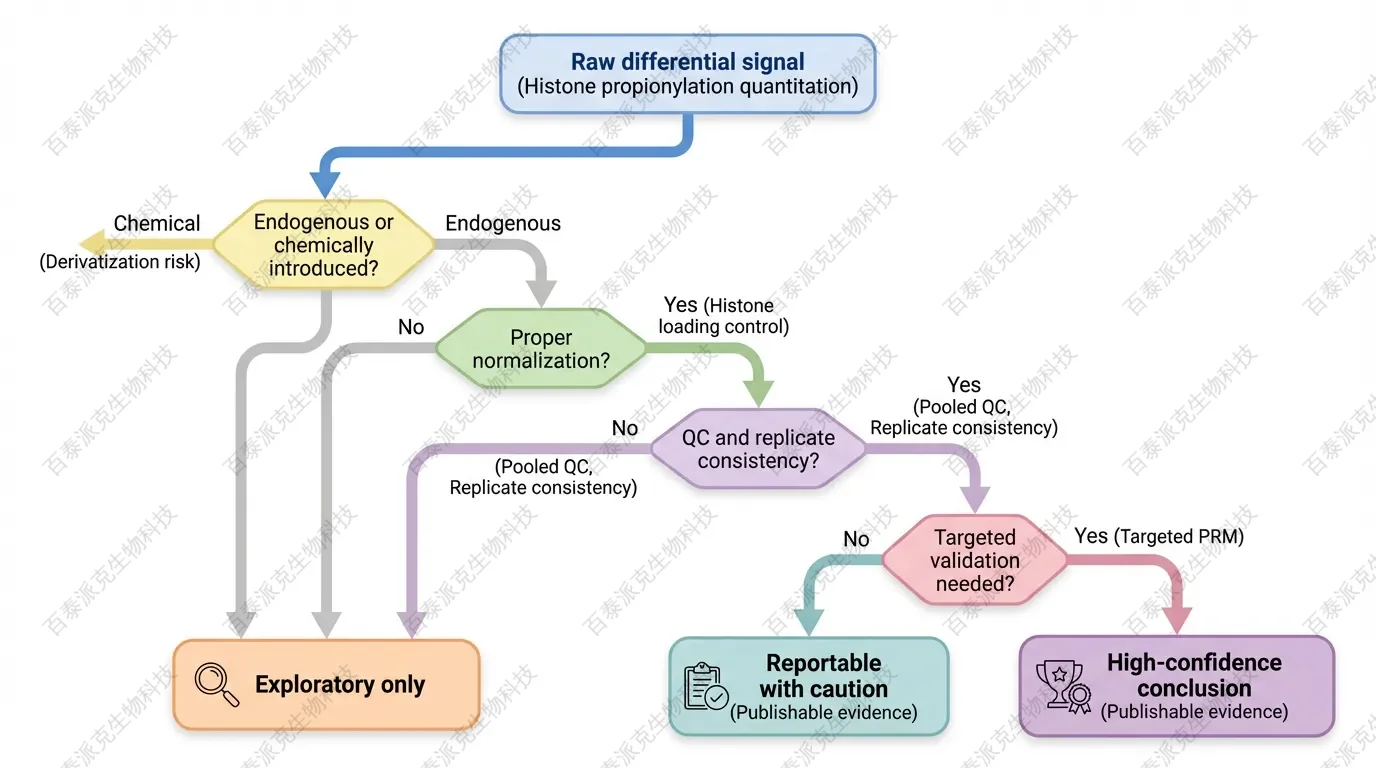
一个更稳妥的判读框架
对组蛋白丙酰化定量结果,建议不要只看单一 fold change,而要同时看四件事:
1. 这个信号是否明确来自天然丙酰化,而不是实验衍生化。
2. 这个位点或这类信号在生物重复中是否方向一致。
3. 归一化方式是否合理,是否排除了装载和批次影响。
4. 是否有正交方法支持,例如靶向质谱、抗体法或功能实验。
主要收益或优势
1. 能把“看到变化”升级成“知道变化发生在哪”
位点级定量让你不再停留在总修饰信号,而是把变化落实到具体组蛋白和具体残基上。
2. 更容易连接代谢状态与表观遗传机制
丙酰化与细胞代谢底物状态密切相关。定量结果越稳,越容易和代谢重编程、染色质开放和基因表达变化建立联系。
3. 更适合后续验证和项目推进
一旦筛出关键位点,后续的 PRM、位点突变、药理干预和多组学联动都会更有方向。
主要限制或权衡
|
难点 |
为什么会出现 |
更稳妥的应对方式 |
|---|---|---|
|
天然丰度低 |
弱信号更容易被背景和漂移放大 |
提前降低样本复杂度,必要时转入靶向验证 |
|
化学衍生化干扰解释 |
经典流程可能引入人工 propionylation |
在方法设计时区分天然与实验修饰 |
|
多修饰共存 |
同一肽段可能有多种 PTM 竞争解释 |
强化谱图复核和搜索策略 |
|
归一化不当 |
不同输入量会扭曲差异结果 |
预先定义归一化与 QC 规则 |
|
批次效应 |
低丰度 PTM 对仪器状态更敏感 |
设置 pooled QC、随机上机与批次校正 |
常见问题(FAQ)
1. 组蛋白丙酰化定量能只做 Western blot 吗?
如果你的目标只是观察总水平趋势,可以;但如果你需要位点级结论或高可信定量,单做 Western blot 不够。
2. discovery LC-MS/MS 的 fold change 能直接写进结论吗?
通常不建议直接这样做。更稳妥的做法是把它当成候选线索,再通过重复验证、靶向质谱或其他正交证据进行确认。
3. 为什么常规 histone propionylation derivatization 会让结果更难解释?
因为它可能在实验过程中人为引入丙酰基,而你的研究问题又恰好是天然丙酰化水平。两者不区分,就会让“定量结果”失去生物学指向性。
4. 什么时候值得做稳定同位素内标?
当你需要跨批次比较、验证少数关键位点,或者希望把方法做成更稳健的长期检测流程时,内标通常非常值得投入。
5. 总水平、位点级和靶向验证三者是什么关系?
它们更像同一项目的三个阶段,而不是彼此替代。很多项目会先用总水平筛查,再做 discovery 找位点,最后用靶向方法把关键结论坐实。
How to order?








