CO-IP和Pull Down比较解析蛋白结构
蛋白质是生物体内重要的功能分子,其结构决定了其功能。因此,了解蛋白质的结构对于理解其功能和参与的生物过程至关重要。在生物药物研究领域,科学家们经常使用不同的方法来解析蛋白质的结构。其中,CO-IP和Pull Down是两种常用的方法,本文将对这两种方法进行比较,探讨其在蛋白结构鉴定中的应用。
一、CO-IP(共免疫沉淀)方法
CO-IP是一种利用抗体与目标蛋白质特异性结合的原理,将目标蛋白质与其相互作用的蛋白质一同沉淀下来的方法。具体步骤如下:
1.细胞裂解:将目标蛋白质所在的细胞裂解,释放出细胞内的蛋白质。
2.抗体结合:将特异性抗体与目标蛋白质结合,形成抗原-抗体复合物。
3.免疫沉淀:将抗原-抗体复合物与蛋白质A/G磁珠结合,通过磁力将复合物沉淀下来。
4.洗涤:用缓冲液洗涤沉淀下来的复合物,去除非特异性结合的蛋白质。
5.蛋白质分离:将洗涤后的复合物进行电泳分离,得到目标蛋白质及其相互作用的蛋白质。
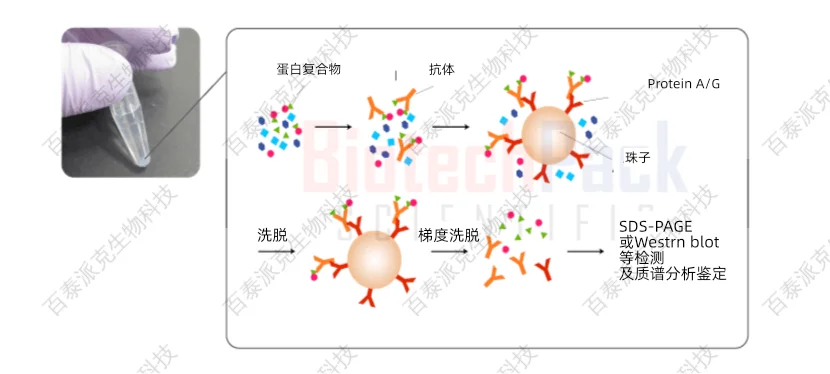
图1
CO-IP方法的优点是可以保留蛋白质的天然结构和相互作用,能够较好地鉴定蛋白质的结构。然而,该方法需要特异性的抗体,且操作复杂,需要较长的时间。
二、Pull Down(下拉法)方法
Pull Down方法是一种利用亲和层析技术,将目标蛋白质与其相互作用的蛋白质一同富集下来的方法。具体步骤如下:
1.目标蛋白质结合:将目标蛋白质与亲和标记(如GST、His等)结合,形成融合蛋白。
2.亲和层析:将融合蛋白与亲和树脂结合,通过重力或离心力将融合蛋白及其相互作用的蛋白质富集下来。
3.洗涤:用缓冲液洗涤富集下来的蛋白质,去除非特异性结合的蛋白质。
4.蛋白质分离:将洗涤后的蛋白质进行电泳分离,得到目标蛋白质及其相互作用的蛋白质。

图2
Pull Down方法的优点是操作相对简单,时间较短,适用于高通量实验。然而,该方法可能会引入亲和标记对蛋白质的结构和功能产生影响,需要谨慎选择亲和标记。
三、CO-IP和Pull Down的比较
CO-IP和Pull Down方法在蛋白结构鉴定中有各自的优缺点,下面进行比较:
1.抗体选择:CO-IP需要特异性的抗体,而Pull Down需要选择合适的亲和标记。抗体的选择和亲和标记的引入都可能对蛋白质的结构和功能产生影响,需要谨慎考虑。
2.操作复杂度:CO-IP操作相对复杂,需要多个步骤和较长的时间;而Pull Down操作相对简单,时间较短,适用于高通量实验。
3.结果解读:CO-IP可以保留蛋白质的天然结构和相互作用,有助于鉴定蛋白质的结构;而Pull Down可能会引入亲和标记对蛋白质的结构和功能产生影响,需要谨慎解读结果。
CO-IP和Pull Down是两种常用的方法,用于解析蛋白质的结构。CO-IP可以保留蛋白质的天然结构和相互作用,适用于鉴定蛋白质的结构;而Pull Down操作相对简单,适用于高通量实验。在选择方法时,需要根据实验目的和需求综合考虑各自的优缺点。未来,随着技术的不断发展,相信会有更多更高效的方法用于蛋白结构鉴定,为生物药物研究提供更多的可能性。
百泰派克生物科技——生物制品表征,多组学生物质谱检测优质服务商
相关服务:
How to order?








