圆二色谱如何揭示蛋白质构象的多样性?
蛋白质是生命体内最重要的分子之一,它们在细胞内发挥着关键的功能。蛋白质的功能与其构象密切相关,而蛋白质的构象又受到其二级结构、折叠状态和构象变化的影响。因此,了解蛋白质的构象对于理解其功能和生物学过程至关重要。在生物制药领域,研究蛋白质构象的多样性对于新药研发和生物医学研究具有重要意义。本文将重点介绍一种常用的生物物理技术——圆二色谱,以及它如何揭示蛋白质构象的多样性。
一、圆二色谱的原理
圆二色谱是一种通过测量蛋白质对圆偏振光的吸收情况来研究其构象的技术。圆偏振光是一种具有特定旋转方向的偏振光,而蛋白质分子对圆偏振光的吸收会导致光的旋转方向发生改变。圆二色谱通过测量蛋白质对圆偏振光的吸收强度和旋光角度的变化,可以获得蛋白质的圆二色谱谱图。
二、圆二色谱如何揭示蛋白质的二级结构?
蛋白质的二级结构是指由氨基酸残基之间的氢键和其他非共价相互作用所形成的局部结构。常见的蛋白质二级结构包括α-螺旋、β-折叠和无规卷曲。圆二色谱可以通过测量蛋白质对圆偏振光的吸收情况来揭示蛋白质的二级结构。
α-螺旋结构对圆偏振光的吸收具有特定的角度依赖性。当圆偏振光的旋转方向与α-螺旋结构的旋转方向一致时,蛋白质会吸收更多的光,产生正的圆二色信号。相反,当圆偏振光的旋转方向与α-螺旋结构的旋转方向相反时,蛋白质会吸收较少的光,产生负的圆二色信号。通过测量不同波长下的圆二色信号,可以确定蛋白质中α-螺旋结构的含量和分布。
β-折叠结构对圆偏振光的吸收也具有特定的角度依赖性。与α-螺旋结构不同的是,β-折叠结构的圆二色信号通常是负的。通过测量不同波长下的圆二色信号,可以确定蛋白质中β-折叠结构的含量和分布。
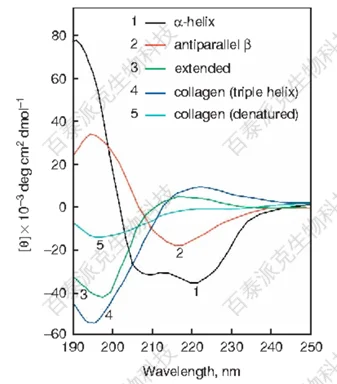
图1
三、圆二色谱如何揭示蛋白质的折叠状态和构象变化?
蛋白质的折叠状态和构象变化对其功能和生物学过程具有重要影响。圆二色谱可以用来研究蛋白质的折叠状态和构象变化。
当蛋白质发生折叠时,其二级结构的含量和分布会发生变化,从而导致圆二色谱信号的变化。通过比较已知折叠状态的蛋白质和未折叠状态的蛋白质的圆二色谱信号,可以确定蛋白质的折叠状态。
此外,蛋白质的构象变化也可以通过圆二色谱来研究。当蛋白质发生构象变化时,其二级结构的含量和分布也会发生变化,从而导致圆二色谱信号的变化。通过比较不同构象的蛋白质的圆二色谱信号,可以确定蛋白质的构象变化。
四、圆二色谱在蛋白质与其他分子相互作用研究中的应用
蛋白质与其他分子的相互作用对于生物学过程和药物研发具有重要意义。圆二色谱可以用来研究蛋白质与其他分子的相互作用方式。
当蛋白质与其他分子结合时,其二级结构的含量和分布会发生变化,从而导致圆二色谱信号的变化。通过比较蛋白质与不同分子结合后的圆二色谱信号,可以确定蛋白质与其他分子的相互作用方式。
五、圆二色谱在生物制药领域的应用前景
圆二色谱在生物制药领域具有广阔的应用前景。通过研究蛋白质的构象多样性,圆二色谱可以为新药研发和生物医学研究提供有力支持。
在新药研发中,圆二色谱可以用来研究药物与蛋白质的相互作用方式,从而帮助优化药物设计和筛选。此外,圆二色谱还可以用来研究药物的药效和毒性,为药物的安全性评估提供重要信息。
在生物医学研究中,圆二色谱可以用来研究蛋白质的结构和功能,从而深入理解生物学过程的机制。通过研究蛋白质的构象多样性,圆二色谱可以揭示蛋白质在疾病发生和发展中的作用,为疾病的诊断和治疗提供新的思路和方法。
圆二色谱是一种重要的生物物理技术,可以用来研究蛋白质的构象多样性。通过测量蛋白质对圆偏振光的吸收情况,圆二色谱可以揭示蛋白质的二级结构、折叠状态和构象变化,以及蛋白质与其他分子的相互作用方式。这些信息对于理解蛋白质的功能和生物学过程具有重要意义。在生物制药领域,圆二色谱的应用前景广阔,将为新药研发和生物医学研究提供有力支持。
百泰派克生物科技——生物制品表征,多组学生物质谱检测优质服务商
相关服务:
How to order?








